福祉機器の国際標準及び各国の規格・安全基準等の概要について
(「第8回勉強会資料(国立障害者リハビリテーションセンター研究所 福祉機器開発部長 井上 剛伸 氏)」より)
○安全基準・・・(ISO/IEC ガイド51・JIS Z8051“安全側面-規格への導入指針”)
安全:受容できないリスクがないこと
リスク:危害の発生確率及びその危害の程度の組み合わせ
※「消費生活用製品安全法」が改正され、製品事故情報の報告・公表制度が開始された。
対象製品には電動ベッドや電動車いすも含まれており、これまで死亡事故の公表が行われ、メーカーの自主回収や改善等につながっている。支援機器の重大事故に対する処置として、法に基づき公表等が行われることとなったことは利用者にとっても望ましいことである。
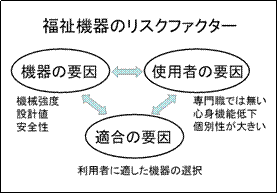
○福祉機器の国際標準(機械要因)国際規格:ISO(国際標準化機構)/IEC(国際電気標準会議)
・ 欧州規格:CEN(欧州標準化委員会)/CENELEC(欧州電気標準化委員会)
・ 各国工業規格:JIS(日本),DIN(ドイツ),ANSI/RESNA(アメリカ),他
・ 各国では支給するにあたって、工業規格にプラスした形で基準を設けている
(スウェーデンでは障害研究所が試験評価し、合格したものを支給リストへ掲載)
○支給制度と安全基準の考え方ISO,JIS等の工業規格は第1段階の基準として考えられる
・ 支給する立場からは、利用者の個別性や障害を十分考慮した安全基準が必要
・ JISとの協調か独自基準の策定か意見のあるところ
・ 工業規格にプラスする形で、臨床評価及び個別適合評価等の検討が必要
※ 国際標準やJIS規格、安全対策等については、経済産業省をはじめとした関係府省庁との連携が重要となる。